You are looking for information, articles, knowledge about the topic nail salons open on sunday near me 옥텟 on Google, you do not find the information you need! Here are the best content compiled and compiled by the https://toplist.maxfit.vn team, along with other related topics such as: 옥텟 옥텟 바이트, 옥텟규칙, 옥텟 월렛, 네트워크 옥텟, 옥텟규칙 예외, 옥텟 서비스, IP 옥텟, 옥텟규칙 위반
옥텟(octet)은 컴퓨팅에서 8개의 비트가 한데 모인 것을 말한다. 초기 컴퓨터들은 1 바이트가 꼭 8 비트만을 의미하지 않았으므로, 8비트를 명확하게 정의하기 위해 옥텟이라는 용어가 필요했던 것이다.
옥텟 (컴퓨팅) – 위키백과, 우리 모두의 백과사전
- Article author: ko.wikipedia.org
- Reviews from users: 29387
Ratings
- Top rated: 5.0
- Lowest rated: 1
- Summary of article content: Articles about 옥텟 (컴퓨팅) – 위키백과, 우리 모두의 백과사전 Updating …
- Most searched keywords: Whether you are looking for 옥텟 (컴퓨팅) – 위키백과, 우리 모두의 백과사전 Updating
- Table of Contents:
예외[편집]
일반[편집]
각주[편집]

옥텟 (컴퓨팅) – 위키백과, 우리 모두의 백과사전
- Article author: medium.com
- Reviews from users: 13788
Ratings
- Top rated: 3.1
- Lowest rated: 1
- Summary of article content: Articles about 옥텟 (컴퓨팅) – 위키백과, 우리 모두의 백과사전 서버를 구축하기 위해 AWS(Amazon Web Service)를 이용하고 결제 시스템 구축을 위해 Paypal을 활용하는 것처럼 옥텟은 블록체인 지갑 구축과 서비스 … …
- Most searched keywords: Whether you are looking for 옥텟 (컴퓨팅) – 위키백과, 우리 모두의 백과사전 서버를 구축하기 위해 AWS(Amazon Web Service)를 이용하고 결제 시스템 구축을 위해 Paypal을 활용하는 것처럼 옥텟은 블록체인 지갑 구축과 서비스 …
- Table of Contents:
예외[편집]
일반[편집]
각주[편집]

옥텟 규칙(octet rule) | 과학문화포털 사이언스올
- Article author: www.scienceall.com
- Reviews from users: 29447
Ratings
- Top rated: 4.3
- Lowest rated: 1
- Summary of article content: Articles about 옥텟 규칙(octet rule) | 과학문화포털 사이언스올 옥텟 규칙은 분자를 이루는 각각의 원자는 최외각 껍질에 8개가 들어갔을 때 가장 안정된 상태라고 하는 화학 이론이다. 이는 탄소·산소·할로겐 원소 … …
- Most searched keywords: Whether you are looking for 옥텟 규칙(octet rule) | 과학문화포털 사이언스올 옥텟 규칙은 분자를 이루는 각각의 원자는 최외각 껍질에 8개가 들어갔을 때 가장 안정된 상태라고 하는 화학 이론이다. 이는 탄소·산소·할로겐 원소 … 과학의 모든 것! 과학 학습, 과학 체험, 과학 문화의 모든 것 사이언스올!옥텟 규칙은 분자를 이루는 각각의 원자는 최외각 껍질에 8개가 들어갔을 때 가장 안정된 상태라고 하는 화학 이론이다.옥텟규칙
- Table of Contents:

옥텟
- Article author: www.terms.co.kr
- Reviews from users: 6786
Ratings
- Top rated: 3.1
- Lowest rated: 1
- Summary of article content: Articles about 옥텟 컴퓨터에서의 옥텟은 8 비트의 배열을 말한다. 그러므로, 옥텟 한 개는 일반적으로 8 비트로 구성된 한 바이트와 같다. 그러나, 모든 컴퓨터 시스템이 8 비트를 1 … …
- Most searched keywords: Whether you are looking for 옥텟 컴퓨터에서의 옥텟은 8 비트의 배열을 말한다. 그러므로, 옥텟 한 개는 일반적으로 8 비트로 구성된 한 바이트와 같다. 그러나, 모든 컴퓨터 시스템이 8 비트를 1 …
- Table of Contents:

옥텟규칙 예외와 위반(violation of the octet rule) : 네이버 블로그
- Article author: blog.naver.com
- Reviews from users: 34891
Ratings
- Top rated: 4.2
- Lowest rated: 1
- Summary of article content: Articles about 옥텟규칙 예외와 위반(violation of the octet rule) : 네이버 블로그 옥텟규칙(octet rule)이란 최외각전자(원자가전자)가 완전히 채워진 즉, 8개가 될때 원소는 가장 안정하다는 규칙입니다. 원소들의 전자배치는 최외각 … …
- Most searched keywords: Whether you are looking for 옥텟규칙 예외와 위반(violation of the octet rule) : 네이버 블로그 옥텟규칙(octet rule)이란 최외각전자(원자가전자)가 완전히 채워진 즉, 8개가 될때 원소는 가장 안정하다는 규칙입니다. 원소들의 전자배치는 최외각 …
- Table of Contents:
블로그
악성코드가 포함되어 있는 파일입니다
작성자 이외의 방문자에게는 이용이 제한되었습니다
Octet – Blockchain Developer Tool
- Article author: octet.im
- Reviews from users: 46290
Ratings
- Top rated: 3.1
- Lowest rated: 1
- Summary of article content: Articles about Octet – Blockchain Developer Tool Blockchain-as-a-Service. Cloud-based Blockchain Infrastructure. Prove Blockchain Developer Tools, Octet. BaaS Service. …
- Most searched keywords: Whether you are looking for Octet – Blockchain Developer Tool Blockchain-as-a-Service. Cloud-based Blockchain Infrastructure. Prove Blockchain Developer Tools, Octet. BaaS Service. Blockchain-as-a-Service. Cloud-based Blockchain Infrastructure. Provide Blockchain Developer Tools, Octet. BaaS ServiceHexlant, Blockchain-as-a-Service, Blockchain Service Network, BaaS, Blockchain Development, Custody, Security, Infura, Bitgo, Hexlant Octet
- Table of Contents:
The Fastest Way toUnlock Web3
Why Octet
Octet is built for all developers
Customer Success Story
Frequently Asked Questions
User Guide

금성출판사 :: 티칭백과
- Article author: dic.kumsung.co.kr
- Reviews from users: 6270
Ratings
- Top rated: 4.2
- Lowest rated: 1
- Summary of article content: Articles about 금성출판사 :: 티칭백과 옥텟 규칙 octet rule. 트위터 페이스북 메일 프린트 url복사. 원자는 최외각 껍질이 완전히 채워지거나 전자 8 … …
- Most searched keywords: Whether you are looking for 금성출판사 :: 티칭백과 옥텟 규칙 octet rule. 트위터 페이스북 메일 프린트 url복사. 원자는 최외각 껍질이 완전히 채워지거나 전자 8 …
- Table of Contents:

See more articles in the same category here: toplist.maxfit.vn/blog.
위키백과, 우리 모두의 백과사전
옥텟(octet)은 컴퓨팅에서 8개의 비트가 한데 모인 것을 말한다. 초기 컴퓨터들은 1 바이트가 꼭 8 비트만을 의미하지 않았으므로, 8비트를 명확하게 정의하기 위해 옥텟이라는 용어가 필요했던 것이다. 그러나 요즘에는 바이트하고 같은 의미가 되어 8비트를 의미하는 옥텟은 더 이상 일반적으로 사용되지는 않는다.[1][2]
예외 [ 편집 ]
허가 권한 옥텟(permission octet)이라는 용어는 유닉스 계열 플랫폼의 수많은 파일 시스템의 기본 허가 비트 (읽기, 쓰기, 실행)에 쓰이기도 한다. 이 3개의 비트는 8개의 다른 값을 대표하므로 8진법으로 표기하기도 한다. “permission triplet”이라는 표현도 사용한다.
일반 [ 편집 ]
옥텟은 1998년에 국제 전기 표준 회의가 SI 접두어 또는 이진 접두어에 쓸 수 있게 표준화하였다. 바로 아래에는 이진법으로 표기한 것이다.
키비(kibi): « ki lo bi nary »
lo nary » 메비(mebi): « me ga bi nary »
ga nary » 기비(gibi): « gi ga bi nary »
ga nary » 테비(tebi): « tera binary »
1 kibioctet (Kio) = 210 옥텟 = 1,024 옥텟 1 mebioctet (Mio) = 220 옥텟 = 1,024 Kio = 1,048,576 옥텟 1 gibioctet (Gio) = 230 옥텟 = 1,024 Mio = 1,073,741,824 옥텟 1 tébioctet (Tio) = 240 옥텟 = 1,024 Gio = 1,099,511,627,776 옥텟 1 pebioctet (Pio) = 250 옥텟 = 1,024 Tio = 1,125,899,906,842,624 옥텟 1 exbioctet (Eio) = 260 옥텟 = 1,024 Pio = 1,152,921,504,606,847,000 옥텟 1 zebioctet (Zio) = 270 옥텟 = 1,024 Eio = 1,180,591,620,717,411,300,000 옥텟 1 yobioctet (Yio) = 280 옥텟 = 1,024 Zio = 1,208,925,819,614,629,200,000,000 옥텟
십진법의 사용은 다음과 같다:
1 kilooctet (ko) = 103 옥텟 = 1,000 옥텟 1 megaoctet (Mo) = 106 옥텟 = 1,000 ko = 1,000,000 옥텟 1 gigaoctet (Go) = 109 옥텟 = 1,000 Mo = 1,000,000,000 옥텟 1 teraoctet (To) = 1012 옥텟 = 1,000 Go = 1,000,000,000,000 옥텟 1 petaoctet (Po) = 1015 옥텟 = 1,000 To = 1,000,000,000,000,000 옥텟
옥텟규칙 예외와 위반(violation of the octet rule)
옥텟규칙(octet rule)이란 최외각전자(원자가전자)가 완전히 채워진 즉, 8개가 될때 원소는 가장 안정하다는 규칙입니다. 원소들의 전자배치는 최외각전자가 8개인 원소들도 있지만(이 원소들은 비활성기체로써 안정하므로 결합하려 하지않으려함), 대부분은 그렇지 못하므로(1~7개) 이들은 원소들간의 결합을 통해서 최외각전자가 8개가 되도록 결합하려 합니다.
하지만 일부의 원소들간의 결합은 옥텟규칙을 지키지 못하는 경우도 있습니다. 옥텟규칙을 어기는 이유는 결합하려는데 전자의 수가 8개 보다 적거나 많기 때문입니다. 원소들간의 결합형태는 너무도 많고 다양하므로 최선보다는 차선을 선택한 것이며, 옥텟규칙을 어기더라도 상대원소(주로 가벼운 원소)의 옥텟규칙은 지켜주는 경우가 대부분입니다. 즉, 모두 지키지는 못하더라도 어느 한쪽은 옥텟규칙을 지키고 있게 됩니다. 옥텟규칙을 어기는 결합은 불완전한 결합이므로 안정한 상태는 아닙니다.
최외각의 전자수는 2개와 8개일때 가장 안정하므로, 수소와 같은 원소들은 헬륨과 같은 형태인 최외각전자수를 2개로 맞추는 듀엣규칙(duet rule, duplet rule)을 따릅니다. 따라서 H가 단독적으로 있을때보다 H-H (H 2 )의 결합을 한 상태가 안정하므로 자연계의 대부분의 수소 등은 이상태(이원자분자)로 존재합니다. H 2 O의 경우 듀엣규칙과 옥텟규칙이 같이 존재하는 안정한 결합(공유결합)을 합니다. 수소와 마찬가지로 산소(O)와 질소(N) 등도 단독적으로 존재하지 않고, 옥텟규칙에 따른 결합을 하는 것이 안정하므로 자연계에 존재하는 산소와 질소의 형태는 대부분 O 2 , N 2 의 형태입니다.
<듀엣 규칙, 옥텟 규칙, 18전자 규칙>
■ 옥텟규칙의 이해
위의 그림은 염화칼슘의 결합구조를 나타낸 것입니다. 한개의 칼슘과 두개의 염소는 2X2의 전자를 공유하며, 염소는 전자 8개의 안정한 결합 그리고 칼슘은 전자 4개의 옥텟규칙을 어기는 결합을 하고 있습니다.
하지만 칼슘은 옥텟규칙을 어기지 않았습니다. 왜냐하면 실제의 결합 구조는 아래와 같습니다. 염화칼슘이 공유결합이었다면 위와 같았겠지만, 염화칼슘은 공유결합이 아니라 이온결합을 하고 있습니다.
공유결합은 전자를 서로 공유하는 것이지만, 이온결합은 한쪽(금속)이 전자를 잃거나 또는 다른쪽(비금속)이 전자를 얻어가는 것입니다. 따라서 아래 그림처럼 염소와 칼슘은 모두 옥텟규칙을 지키고 있습니다.
이온결합의 경우는 대부분 원자가전자수의 +와 -의 상대적인 계산에 의한 결합이므로 웬만해서는 위와 같은 형식의 구조를 가지는 경우가 대부분입니다. 전자를 잃었거나 얻어서 이온상태이지만 옥텟규칙을 지키기 위한 행위였습니다.
■ 공명구조는 옥텟규칙 위반인가?
<여기서 +와 -의 표시는 전자의 유무가 아니라, +극성과 -극성을 의미함(하나의 자석임). 상대적으로 비공유 전자쌍이 적은 곳이 +극성을 띠게됨. 좌우 공명을 하므로 -극성이 상대적으로 서로 바뀜.>
위의 결합은 모두 공유결합인데, 일산화질소(NO)는 질소가 최외각전자가 7개여서 옥텟규칙을 위반하고 있습니다. 따라서 일산화질소는 불안정하며 해로운 기체입니다. 일산화질소는 좀더 안정한 구조인 이산화질소(NO 2 )로 바뀌려 합니다. 이때 일산화질소는 대기중의 산소(O 2 )에서 산소 한분자를 뺏어오며 자신과 결합합니다. 그러면서 이산화질소가 됩니다. 이산화질소 역시 옥텟규칙을 위반하고 있는 결합입니다. 하지만 이산화질소가 일산화질소보다 안정한 이유는 일산화질소는 할 수 없는 공명을 하는 공명구조(resonance structure)이기 때문입니다. 이렇게 이산화질소는 양쪽의 산소가 공명함으로써 질소 자신은 자기가 마치 최외각전자가 8개인 것 같은 착각을 가지게 합니다(어차피 7개임).
일산화질소로부터 산소 한개를 빼앗긴 산소(O)분자는 라디칼산소로써 안정한 산소기체(O 2 )와 결합하여 해로운 오존(O 3 )을 만듭니다. 오존은 옥텟규칙을 지키면서 공명하고 있습니다.
오존은 옥텟규칙을 지키고 있지만 굳이 공명하는 이유는, 좌우의 안정한 전자배치뿐만아니라, 공명을 하지 않으면 위의 그림처럼 옥텟규칙을 깨는 엉뚱한 결합구조가 나타나기 때문입니다. 이것은 위의 이산화질소가 공명하는 이유이기도 합니다. 이산화질소는 공명을 하고 있으면서도 옥텟규칙을 어기고 있지만, 공명조차하지 않으면 그보다 더욱 이상한 구조가 되어 버리기 때문입니다. 공명자체가 분자의 극성을 일으키기도 합니다. 위의 오존도 극성을 가지겠지만 옥텟규칙은 어겼습니다.
결국 공명구조는 옥텟규칙을 구조에 따라 어기는 결합도 있고, 지키는 결합(또는 옥텟규칙을 지키기 위해 공명)도 있습니다. 공명도 아무 결합이나 할 수 있는 것은 아니고, 전자배치의 좌우 배치가가 균일할 수 있고, 분자량 등 균형이 잡혀 있을때만 할 수 있습니다(물리적으로 볼때 서로의 진동수가 맞아야함).
■ 배위결합은 옥텟규칙 위반인가?
배위결합은 변칙적인 공유결합의 일종입니다. 변칙적인 이유는 전자를 서로 공유하는 것이 아니라 한쪽에서 전자를 꾸어오기 때문입니다. 그림1과 그림2는 같은 의미인데, 표현을 다르게 했을 뿐입니다. 그림1에서 배위결합은 ●●로 표기하고 공유결합은 ●X로 표기하였습니다. 그림2에서 질소가 전자가 없는 수소이온(+)에게 전자를 빌려주어 서로 결합합니다. 질소가 결합참여전자가 없는 홑전자쌍(비공유전자쌍)상태보다 차라리 결합하고 있는 상태가 안정하므로 수소양이온에게 전자를 꿔주면서 결합에 참여시킵니다(암모늄이온은 수용액에서만 존재하므로 어쩔수 없는 선택이기도 함). 따라서 질소 입장에서는 결합의 전과 후가 옥텟규칙에 위반되지 않았으므로 크게 손해본 것은 없고, 오히려 덕분에 수소양이온이 듀엣규칙을 지키게 되었습니다.
■ 혼성오비탈은 옥텟규칙 위반인가?
물(H 2 O)은 공유결합인데, 혼성오비탈로 표현할 수도 있습니다. 물은 Tetrahedral한 4면체 구조로 볼 수 있습니다. Tetrahedral한 혼성오비탈의 4면체로 표현하기 위해서는 고립전자쌍을 들뜨게하여 결합참여전자 4쌍을 가지는 sp3 사각형 구조를 가지게 표현하게 됩니다. 그렇다고 하더라도 옥텟규칙을 어기지는 않습니다. 모든 혼성오비탈이 옥텟규칙을 어기는 것은 아닙니다.
하지만 여기서 주의할 점이 있습니다. 수소의 듀엣결합을 옥텟규칙으로 볼 수 있냐? 없냐? 입니다. 왜냐하면 옥텟규칙은 어쨋든 8개의 전자를 의미하기 때문입니다. 따라서 엄밀히 말하면 물은 옥텟규칙을 어기는 결합입니다. 하지만 경우에 따라서는 수소 자체가 옥텟규칙을 따르는 것은 불가능 하기 때문에 수소는 무시하고 산소를 기준으로 봐서 물은 옥텟규칙을 따른다고 보는 것이 보편적인 관점입니다.
혼성오비탈의 경우도 수소(H)가 결합에 참여된 경우는 대부분 넓은의미(확장된)의 옥텟규칙을 따르지만, 수소(H)가 결합에 참여되지 않은 경우에는 대부분 옥텟규칙을 따르지 않기 때문입니다.
<이산화탄소(CO 2 )는 비극성공유결합, 물(H 2 O)은 극성공유결합>
<이온결합은 극성이 없음. 옥텟규칙을 모두 지키더라도 상대적인 전자의 크기에 차이가 발생하면 극성을 가짐. 극성을 가지게 되면 전자기장에 반응을 함.>
결합분자간의 전기음성도 차이가 가장 큰것은 이온결합입니다. 하지만 전자를 공유하는 것이 아니라 서로 주고 받아서 비공유전자쌍 없이 옥텟규칙을 채우는 개념이기 때문에 극성이 없습니다. 그러므로 이온결합은 +와 -의 전기적인 특성이 잠재되어 있을뿐, 자석의 기능(자기쌍극자)은 없다는 것입니다.
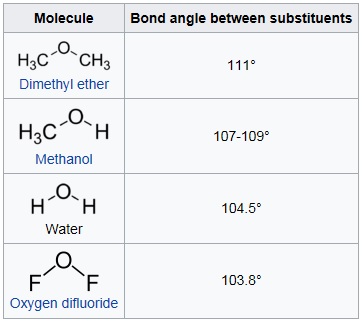
루이스구조식은 장점도 있지만 화합물들의 정확한 구조를 표현하는데 한계가 있습니다. 혼성오비탈 sp3의 정사면체 형태를 취하는 메탄과 물의 경우, 정사면체는 중심으로부터 109.5˚의 각도를 가지므로 메탄의 경우 그러하지만, 물은 수소간의 104.5˚의 각도를 가지고 있습니다. 물은 공유전자쌍 2개와 비공유전자쌍 2개의 반발력이 서로 다르므로 상대적으로 수소간의 결합 각이 물리적으로 위축되었다고 봅니다.
<다양한 화합물들의 서로 다른 결합각>
<그림출처 : Bent's rule - 위키백과>
이를 원자가껍질 전자쌍 반발 이론(Valence shell electron pair repulsion theory : VSEPR theory)이라고 합니다.
■ 옥텟규칙 위반
옥텟규칙을 위반하는 결합들은 대부분 구조적으로 최외각전자수 8개를 맞출 수 없는 경우가 대부분입니다.
베릴륨은 최외각전자수가 4개이므로 옥텟규칙을 위반합니다. 염화베릴륨은 금속원소와 비금속원소가 결합한 구조입니다. 당연히 이온결합이므로 염화칼슘의 경우와 마찬가지로 옥텟규칙을 지키거나 해당되지 않는다고 볼 것 같지만, 염화베릴륨은 이온결합보다는 전자를 공유하는 공유결합으로 보는 것이 보편적입니다.
보통 공유결합과 이온결합의 구분을 원소간의 전기음성도 차이가 1.7을 기준으로 하기도 하는데, 베릴륨과 염소는 1.7이내입니다. 즉, 베릴륨과 염소는 전기음성도가 둘다 높고 차이가 크지 않다는 것입니다. 공유결합간에서도 극성결합과 비극성결합이 있는데, 극성공유결합이 되기위해서는 전기음성도의 차이가 0.5~1.7이어야 하고, 0.4이하는 비극성공유결합이 됩니다.
붕소는 최외각전자수가 3개이며, BF 3 는 결합전자가 6개이므로 옥텟규칙을 위반합니다.
질소의 원자가 전자가 7개입니다.
황의 원자가전자가 10개입니다.
기존 오비탈의 관점으로는 황(S)은 2개의 전자만을 결합에 참여시킬 수 있지만, 확장된 오비탈(혼성오비탈)에서는 6개의 전자가 결합에 참여할 수 있습니다. 혼성오비탈이 옥텟규칙과 연관이 있는 것은 아니고, 혼성오비탈을 통해 전자배치를 바꿔 황의 전자 6개를 다른 원자들과 결합에 전부 참여시킵니다. 황의 입장에서 결합해야하는 불소의 원자가 많기 때문입니다.
옥텟규칙을 어기는 원소들의 결합은 대부분 혼성오비탈 구조를 가지고 있습니다.
옥텟규칙을 어기는 원소 또는 결합의 특징은
1. 홀수의 전자를 가지는 원소 ex) BF 3
2. 구조적으로 전자수가 모자른 결합 ex) BeH 2
3. 확장된 원자가 전자수 ex) 전이금속화합물
3주기이상의 원소(Si, Cl, S, P…, 3d오비탈로 확장시켜 채울 수 있는)들이 결합에 참여하는 경우에는 원자가 전자수가 10개 또는 12개인 경우가 있는데, 이를 루이스전자식으로 설명하기에는 역부족이지만, 혼성오비탈은 참여전자의 수를 확장시킴으로써 10개 또는 12개의 전자도 결합에 참여할 수 있습니다. 이경우 중심원소의 전기음성도보다 중심원소 주변의 원소들이 질량수는 작지만 전기음성도가 더 큽니다. 또한 결합참여 전자수가 8개가 채안되는 결합의 경우에도 확장된 옥텟규칙이 적용됩니다. 이것이 가능한 이유는 중심원자가 3s, 3p 궤도함수 외에 3d 궤도함수가 존재하기 때문입니다.
새로운 이론들은 duodectet rule (12 electrons)의 12개의 원자가전자수를 설명하며, 전이금속들은 더 많은 전자가 결합할 수 있는데, 18 electron rule을 따르기도 합니다. 전이금속이 주변에 결합해야하는 원소가 많기 때문에 오비탈 배치를 바꿔 원자가전자를 확장시킵니다.
전이금속인 철을 포함하는 이철 노나카보닐은 옥텟규칙은 어겼습니다만 18전자규칙을 지킵니다.
그러나 확장된 옥텟규칙은 원소들이 옥텟규칙을 일부러 안따르는 것이 아니라 따를 수 없는 상황이기 때문이라는 가능성과 한계가 공존하기도 합니다. 원소들은 옥텟규칙과 옥타브규칙이라는 간격과 주기성을 가지고 있기 때문에 프랙탈 시스템이라는 자유와 규제가 공존하기 때문입니다.
원소들은 전자가 많으면 많은대로, 적으면 적은대로 자신의 오비탈 구조를 깨뜨려서라도 상대원소의 안정성을 지켜주려 합니다. 특히 옥텟규칙에 넘어서는 전자가 필요할때 중심 원소들은 가장 많이 망가지는데, 전자껍질 안쪽의 안정한 내핵 전자들까지 꺼내서 결합에 참여시켜 상대적으로 더 전기음성도가 큰 외각 원소들의 안정성을 먼저 우선시 합니다.
듀엣규칙과 옥텟규칙이 왜 안정할 수 있는지는 동양철학을 통해 확인할 수 있습니다. 현대화학은 사상체질과 팔상체질의 원리가 본의아니게 담겨 있습니다.
<그림출처>
옥텟 규칙
금속 원자들은 전자를 잃고 18족 원소와 같이 마지막 전자 껍질의 전자 수가 8 개가 되려는 경향성을 갖는다. 또한 비금속 원자들은 전자를 얻어 마지막 전자 껍질의 전자 수가 8 개가 되려고 하는데 이러한 경향성을 옥텟 규칙이라고 한다.
원자들이 옥텟 규칙에 따르는 이유는 18족 원소들의 안정성에서 찾을 수 있다. 18족 원소들은 마지막 전자 껍질의 전자 수가 8 개(헬륨은 2 개)로 매우 안정한 상태를 유지하고 있다. 18족 원소들은 매우 안정하기 때문에 다른 물질과 거의 반응하지 않아 천연 상태에서도 일원자 분자의 형태로 발견된다.
나트륨은 마지막 전자 껍질의 전자 수가 1 개이고 그 안쪽 껍질의 전자 수는 8 개이다. 따라서 나트륨은 전자를 하나 잃어서 +1가의 양이온이 되면 마지막 전자 껍질의 전자 수가 18족 원소와 같이 8 개가 되므로 매우 안정해진다. 또한 염소는 마지막 전자 껍질의 전자가 7 개이므로 전자 하나를 얻어서 -1가의 음이온이 되면 마지막 전자 껍질의 전자가 8 개가 되어 매우 안정한 상태가 된다.
So you have finished reading the 옥텟 topic article, if you find this article useful, please share it. Thank you very much. See more: 옥텟 바이트, 옥텟규칙, 옥텟 월렛, 네트워크 옥텟, 옥텟규칙 예외, 옥텟 서비스, IP 옥텟, 옥텟규칙 위반
